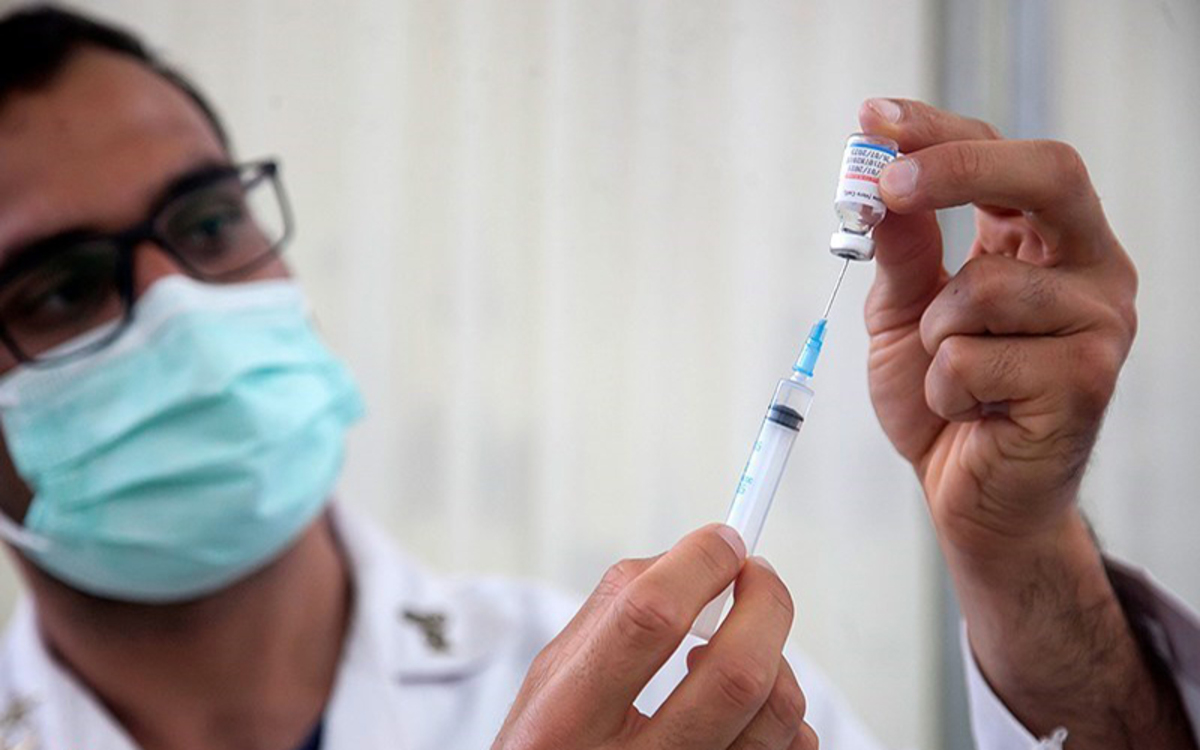
به گزارش بخش اجتماعی سایت خبرمهم، مدیر پروژه واکسن فخرا گفت: واکسنسازهای داخلی که الان در مرحله کارآزمایی بالینی هستند دچار چالش شدهاند و روند مطالعه کارآزمایی بالینی کند شده است.«احمد کریمی» مدیر پروژه واکسن فخرا، در ارتباط با برخی گزارشها مبنی بر کاهش استقبال از مطالعات بالینی واکسنهای داخلی گفت: بالاخره با حجم واکسیناسیونی که در کشور انجام شده که البته خوب است و ما از آن ناراضی نیستیم، تعداد داوطلبان کم شده است. درحال حاضر سن واکسیناسیون از ۱۲ سال به بالا اعلام شده و همه میتوانند واکسن بزنند و طبیعتا انگیزه برای شرکت در مطالعات کم شده است و به همین دلیل واکسن سازهای داخلی که الان در مرحله کارآزمایی بالینی هستند دچار چالش شدهاند و روند مطالعه کارآزمایی بالینی کند شده است.
او افزود: ما توقع داشتیم بین ۱۰۰۰ تا ۱۵۰۰ داوطلب در روز داشته باشیم، اما این عدد به حدود ۱۰۰ نفر رسیده است و از آنجا که در فاز سه حجم نمونه باید زیاد باشد، عملا چالش ایجاد شده است. البته الحمدالله با مساعدت معاونت بهداشتی وزارت بهداشت، روسا و معاونین بهداشتی دانشگاههای علوم پزشکی تهران، ایران، شهید بهشتی، البرز، اصفهان و خراسان رضوی هماهنگی لازم جهت انجام مطالعه در این استانها نیز انجام شد که وضعیت حضور داوطلبان را بهبود بخشیده است.
مدیر پروژه واکسن فخرا گفت: دستوری که وزیر بهداشت قبلی و فعلی داده و در مصاحبهها نیز تاکید کرده بودند این بود که به واکسنهای داخلی همزمان با شروع فاز ۳ مجوز اضطراری داده شود که عملا این اتفاق نیفتاده و مجوز اضطرار مشروط صادر شده است. قید شده گزارش اولیه فاز سه باید ارسال گردد که با توجه به واردات و روند واکسیناسیون عملا رسیدن به این گزارش با کندی مواجه شده است.
کریمی گفت: در دوم شهریور ماه و همزمان با صدور مجوز کمیته اخلاق برای مطالعه فاز ۳، در پی نامه یکی از معاونان در مجموعه وزارت بهداشت به کمیته اخلاق، مجوز تزریق واکسن فخرا نیز به تعویق افتاد و چالش جدی ایجاد شد. الحمدالله با همکاری کمیته اخلاق و سازمان غذا و دارو این مشکل حل شد.
کریمی با اشاره به اینکه مجوز تزریق واکسن فخرا به تعویق افتاد و چالش جدی ایجاد شد، گفت: الحمدالله با همکاری کمیته اخلاق و سازمان غذا و دارو این مشکل حل شد.
او افزود: از مرداد تا به حال یک میلیون دوز تولید کردهایم و از آذر ماه نیز پنج میلیون دوز درماه تولید خواهیم کرد که برای توسعه ظرفیت نیز با شرکت داروسازی ثامن قرارداد همکاری بستهایم و از هفته گذشته نیز اولین بچ را در این شرکت آماده ارائه به بازار کردهایم؛ بنابراین همه زیر ساختهای لازم برای تولید یک محصول کاملا ایرانی را که با همکاری دانشمندان، محققان و شرکتهای دانش بنیان داخلی به ثمر نشسته را در اختیار داریم، اما فعلا در حال برنامهریزی برای توقف تولید هستیم، به این دلیل که تولید کنیم به چه کسی بدهیم؟
کریمی افزود: حتی قولهایی داده شده که پیش خرید انجام شود، اما تا به الان از سمت وزارت بهداشت برای پیش خرید واکسنهای تولیدی نیز اقدامی صورت نگرفته است در صورتی که در جهان دولتها در مرحله تحقیق و توسعه از شرکتها پیش خرید کردند و کشور ما نیز در مرحله تحقیق و توسعه از سبد کواکس پیش خرید کرد و پول واریز کرده بود.
کریمی گفت: همانطور که گفتم ما خوشحال هستیم که با واکسیناسیون عمومی وضعیت جامعه به حالت عادی بازگردد، اما توقع داریم حداقل ۱۰ درصد رقم واردات که به کشورهای مختلف از جمله امارات برای واردات واکسن سینوفارم چینی میدهیم، به واکسن سازهایی که در مرحله مطالعات بالینی به دلیل واردات واکسن به چالش برخوردهاند، اختصاص پیدا کند. بهترین روش این است که حداقلی را از واکسن سازها پیش خرید کنند که این واکسن سازها آرامش خاطری به دست بیاورند، اما مطالعهشان را با همان سرعت کم ادامه بدهند.
او گفت: فرض کنید که مطالعه فاز سه ما با سینوفارم مقایسه میشود. طبیعتا اگر ما مطالعهمان را با سینوفارم مقایسه کردهایم و جوابی در حد سینوفارم یا بهتر بود، آن چیزی که به سینوفارم مترتب میشود برای ما نیز میتواند اتفاق بیافتد. برای مثال با توجه به اینکه فرمولاسیون واکسن سینوفارم برای کودکان و بزرگسالان تفاوتی ندارد، واکسن ما هم میتواند آن رِنج سنی را پوشش بدهد.
او در ادامه گفت: در یک و نیم سال گذشته، کشورهای بزرگ و صنعتی قبل از تحقیقات واکسنها را پیش خرید کردند که این واکسن سازها با خیال راحت کارشان را انجام بدهند. در کشور ما از آغاز این حرف گفته شد، اما هیچوقت این کار را نکردند و از هیچ واکسنسازی پیش خرید انجام نشد. الان هم حرفمان همین است که واکسنهایی که به فاز سه بالینی رسیدهاند را حداقل به اندازه یک و نیم یا دو میلیون دوز پیش خرید کنید. این را هم قول دادهاند، اما هیچ گاه عملی نشده که میتواند بسیار کمک کننده باشد.
کریمی در واکنش به گفته برخی مبنی براینکه به پروژه واکسنهای دولتی هرکدام ۴۰ میلیون دلار پول داده شد که در حکم پیش خرید بوده است، گفت: به ما ده میلیون یورو ارز دولتی داده شد و بقیه واکسنهای داخلی ۴۰ میلیون دلار گرفتند. کمک بلاعوضی به ما داده نشد و ارز دولتی فروخته شده و پول آن هم از ما گرفته شده است.
او درباره وضعیت انتشار نتایج مطالعات واکسن فخرا گفت: مقالههای این پروژه در حال نوشته شدن است که نگارش برخی تمام شده و در ژورنالهای خارجی در حال ادیت است. امیدواریم که پس از اتمام ویرایش به زودی منتشر شود. همه نتایج را به سازمان غذا و دارو نیز اعلام کردیم و هیچ مشکلی از بابت اعلام نتایج نداریم.
کریمی در ارتباط با گروههای غیرمجاز استفاده از این واکسن گفت: درحال حاضر زنان باردار، شیرده و افراد زیر ۱۸ سال و نهایتا افرادی که بیماریهای خاص دارند، مشمول گروه غیرمجاز برای استفاده از این واکسن در فاز مطالعاتی هستند.
او درادامه افزود: ما در فاز یک ۱۳۵ و در فاز دو ۵۰۰ داوطلب داشتیم، براساس نتایجی که به دست آوردیم، این واکسن کاملا بیخطر و کم عارضه بود. ۹۴ درصد افراد دریافت کننده واکسن فخرا افزایش تیتر آنتی بادی داشتند که افزایش حداقل چهار برابری آنتی بادی در ۷۵ این جمعیت مشاهده شد. /ایلنا
تولید «فخرا» متوقف میشود
خبرمهم: همه زیر ساختهای لازم برای تولید یک محصول کاملا ایرانی را که با همکاری دانشمندان، محققان و شرکتهای دانش بنیان داخلی به ثمر نشسته را در اختیار داریم، اما فعلا در حال برنامهریزی برای توقف تولید هستیم، به این دلیل که تولید کنیم به چه کسی بدهیم؟